Возможности медикаментозного обезболивания во время хирургических вмешательств и в ранний послеоперационный период: обновленная информация
М.А. Gurney
Journal of Small Animal Practice (2012)
Анестезиологическое отделение, Northwest Surgeons, Чешир, WA7 3FW
Девизом 2011 г., посвященного борьбе с острой болью во всем мире, было: «Предвидеть, оценивать, облегчать». К последним достижениям в области борьбы с острой болью относятся новые схемы применения широко известных препаратов, новые техники, а также дальнейшее совершенствование наших знаний об оценке боли у животных. Настоящая работа, в которой представлена концепция превентивного обезболивания, написана для закрепления знаний о широко признанной практике превентивного мультимодального обезболивания.
ВВЕДЕНИЕ
2011 г. был признан Международным годом борьбы с острой болью Международной Ассоциации исследования боли (IASP). «Острая боль не является каким-то сложным заболеванием, лечение которого следует предоставлять специалистам по лечению хронических болей, а ситуацией, с которой регулярно сталкиваются все медицинские работники в своей повседневной практике и которую им приходится разрешать» [92]. Несомненно, это утверждение относится и ко всем ветеринарным врачам, занимающимся лечением животных. Девиз Всемирного года борьбы с острой болью «Предвидеть, оценивать, облегчать" - то, что мы все стараемся сделать наилучшим образом по мере своих возможностей. Согласно общепринятым представлениям, боль следует считать пятым жизненным показателем.
Почему необходимо контролировать острую боль?
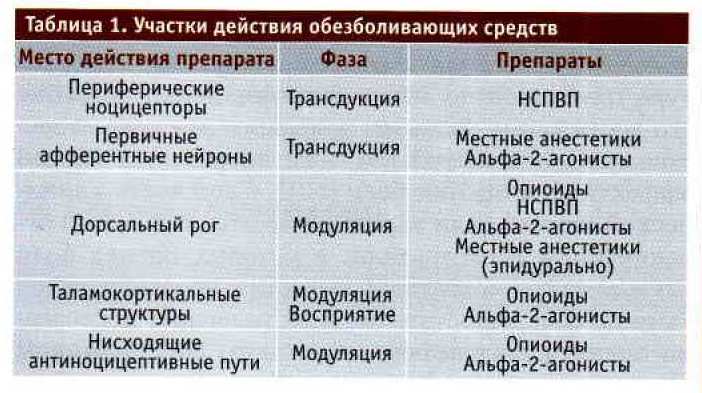
При простом остром состоянии боль обычно пропорциональна раздражителю. Кратковременное повреждение ведет к кратковременному ощущению боли. Если повреждение переходит в следующую стадию, например, при воспалении, индуцированном хирургическим вмешательством, развивается периферическая сенсибилизация, ведущая к устойчивой боли. Это именно та фаза, на которую направлены наши усилия по облегчению или предотвращению боли в результате хирургических вмешательств. Если воспалительное состояние остается без лечения и боль сохраняется, могут произойти изменения в ноцицептивной системе, которые приведут к аномальному кодированию или обработке ноцицептивных раздражителей, например к переходу острой боли в хроническую. На этой стадии тесная корреляция между повреждением и болью исчезает. Обнаружена сильная корреляция между сильной острой послеоперационной болью и развитием хронической боли [63], поэтому клиницисты должны стараться оптимизировать лечение острой боли (рис. 1; табл. 1).
В комментарии эксперта в этом журнале 2010 г. говорится, что благоприятный эффект облегчения боли
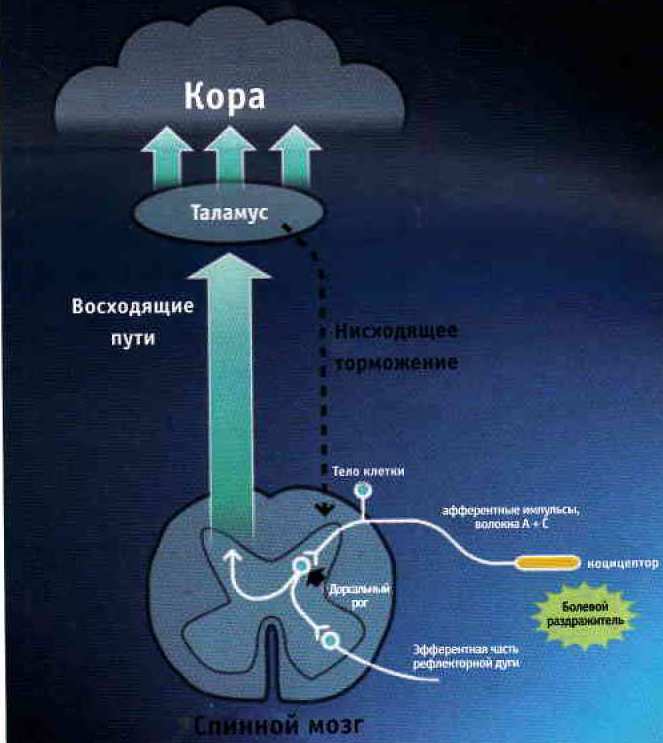
Рис. 1. Нервные пути восприятия боли: нейроанатомические основы боли
Возможности медикаментозного обезболивания во время хирургических вмешательств и в ранний послеоперационный период: обновленная информация
заключается в снижении стрессовой реакции и нарушений снабжения тканей кислородом, сокращении времени нахождения животного в лежачем положении и улучшении подвижности, быстрейшем восстановлении функций, снижении вероятности непроходимости кишечника, облегчении послеоперационного обезболивания и большей удовлетворенности владельцев результатом [55]. Согласно общепринятому мнению в медицине, меры против боли необходимо принимать до операции, используя эффективный превентивный подход, включающий мультимодальное обезболивание (ММО) [46]. Послеоперационная реабилитация, включающая адъювантную терапию, - тнеобходимый компонент борьбы с болью [63]. Обезболивание во время операций и в послеоперационном периоде подробно описано в руководстве по наркозу и обезболиванию собак и кошек BSAVA (2007), а целью настоящего обзора является предоставление практикующим врачам обновленных данных в соответствии с последними достижениями в области медикаментозного лечения острой боли.
Превентивное обезболивание
Превентивное обезболивание определяется как «антиноцицептивное лечение, предотвращающее изменение процесса центральной обработки афферентных импульсов от места повреждения» [46], что практически означает, что начало обезболивания до хирургического разреза помогает лучше контролировать боль после операции, чем при применении той же техники после разреза. Однако на практике простое введение обезболивающих веществ до операции нельзя считать превентивным обезболиванием без учета фармакологических свойств препарата, установление эффективного уровня обезболивания имеет первоочередное значение, и если антиноцицептивные меры перед операцией недостаточны, такой подход нельзя считать превентивным обезболиванием [46]. Например, бупренорфин медленно связывается с рецепторами, и, следовательно, его действие наступает только через 30-45 минут [68, 96], таким образом, очевидно, что при начале хирургического вмешательства ранее этого времени цель превентивного обезболивания не будет достигнута, Сходным образом время достижения максимальной концентрации в плазме после подкожного введения распространенных НСПВП варьирует от 0,5 до 2,5 часа [6, 41], что представляет собой потенциальную брешь в процессе обезболивания (табл. 4).
Концепция превентивного обезболивания остается предметом активных споров среди анестезиологов и специалистов по обезболиванию; однако специалисты соглашаются в том, что опиоиды, действующие на осевую нервную систему (эпидуралъные или спинальные), и системные или эпидуральные антагонисты NMDA (например, кетамин), очевидно, являются наиболее многообещающими средствами для превентивного обезболивания [46], в то время как подобные качества других обезболивающих средств ограничены. Исследования на собаках показали превентивный эффект петидина [56] и карпрофена [57], который подтверждается результатами недавней работы по исследованию бупренорфина на собаках [99]. Эффективная техника превентивного обезболивания требует мультимодального пресечения передачи ноцицептивных импульсов, повышения порога ноцицепции и блокировки или уменьшения активации ноцицеиторов [46]. Эффективнее всего контролировать боль, используя несколько обезболивающих средств, каждое из которых действует на конкретный участок болевого пути, таким образом, результат в меньшей степени зависит от конкретного агента или механизма, эффект усиливается из-за синергического действия, и, кроме того, это позволяет избежать побочных явлений, связанных с высокими дозами отдельных препаратов. У собак и кошек описано синергическое действие альфа-2-агонистов и опиоидов [31, 98] и НСПВП и опиоидов [93, 97, 103]. Необходимым аспектом превентивного обезболивания является то, что обезболивание необходимо продолжать столько, сколько длится болевой раздражитель, вызывающий сенсибилизацию [12], что подчеркивает необходимость в точной оценке боли.
Упреждающее или превентивное обезболивание?
Концепция упреждающего обезболивания относится к времени введения обезболивающих веществ -до или после хирургического разреза. Этот классический превентивный подход в сравнении с обезболиванием после операции подразумевает, что факторы, действующие во время операции, в наибольшей степени способствуют сенсибилизации. Эта концепция была расширена в свете новых знаний о влиянии множества факторов на развитие центральной сенсибилизации; она имеет своей целью ослабление воздействия болевых раздражителей до, во время и после операции и получила название превентивного обезболивания. До настоящего времени неизвестно, каков вклад каждого из трех периодов оперативного вмешательства в развитие центральной сенсибилизации и послеоперационной боли, хотя проводились исследования, подтвердившие благоприятный эффект послеоперационной ноцицептивной блокады в сравнении с блокадой во время операции [28]. Другие исследования показали более эффективное облегчение послеоперационной боли при принятии целенаправленных мер перед операцией [49]. С учетом современных знаний, следует стараться внедрять эффективный план обезболивания на всех стадиях операционного периода в соответствии с подходом "Предвидеть, оценивать, облегчать».
Превентивное обезболивание считается достигнутым при уменьшении послеоперационной боли и/или уменьшении потребности в обезболивающих в течение периода, превышающего длительность действия конкретного препарата, определяемого как 5,5 х время полувыведения препарата [44], а целью превентивного обезболивания является максимальное уменьшение сенсибилизации, индуцированной вредоносными раздражителями, связанными с хирургическим вмешательством, возникающими до, во время и после операции. Если руководствоваться такой пересмотренной концепцией, документальное подтверждение превентивного обезболивания в нашей ветеринарной практике оказывается сложной задачей. Основными средствами ММО считаются опиоиды, НСПБП и местные анестетики. Действие ММО направлено на процессы транедукции, передачи, модуляции и восприятия на разных уровнях нервной системы, таким образом, оптимизация заключается не только в обезболивании в острую фазу, но и в максимальном снижении вероятности развития хронических болей, учитывая растущий интерес к превентивным подходам к обезболиванию, следует обратить наше внимание на оценку и устранение боли, в том числе до операции и во время фазы реабилитации.
Оценка боли
Следует ли добавить понятие «допускать» к трем ключевым подходам «Предвидеть, оценивать, облегчать» при их применении к ветеринарной медицине? Говоря о предвидении боли, мы подразумеваем, что нам известно о болезненности предстоящей операции, При послеоперационном обследовании животного в отсутствии четкой системы балльной оценки боли мы допускаем, что животное испытывает боль. Затем мы допускаем, что обезболивающие средства в нашем арсенале позволяют нам эффективно облегчить боль.
Ранее предполагалось, что овариогистерэктомил болезненнее кастрации, однако доказали этот факт лишь недавно [99]. При сравнении результатов двух исследований, в которых использовались одинаковые методы оценки (оценка боли и оценка порога при механическом воздействии), оценка боли при кастрации оказалась ниже [средний балл по визуальной аналоговой шкале (БАШ) составил 30 в сравнении с 40/100], и при данной операции меньшему числу собак требовалось экстренное обезболивание.
Многие специалисты признают важность качественного обезболивания во время операции; в литературе опубликовано много информации о способах его достижения. Если мы применим это доказательство к нашим пациентам, нам потребуется способ эффективной оценки боли [101]. Сложность клинической оценки боли хорошо известна и является ограничением исследований, в которых оценка боли служит мерой исхода [50]. Известно, что наблюдение само по себе недостаточно и не позволяет достоверно оценить дискомфорт ЖИВОТНОГО [93]. В данном конкретном исследовании на собаках были случаи, в которых полная оценка показывала неконтролируемую боль, требующую дальнейшего обезболивания, однако по результатам только визуального наблюдения эта же боль оценивалась как слабая. Дискомфорт животных не обнаруживался до тех пор, пока проводящий оценку не начинал проводить манипуляции с животным или пальпировать рану. Конечная оценка боли после манипуляций с животным была всегда выше, чем оценка, основанная только на наблюдениях. Этот факт был принят во внимание при разработке современных шкал оценки боли, включающих интерактивный компонент [37].
Отсутствие легко распознаваемых симптомов боли может привести к ложному заключению о том, что животное не испытывает боли либо, напротив, испытывает мучительную боль. Несмотря на сложность оценки боли, была разработана система оценки острой боли для собак, прошедшая проверку на соответствие содержания, возможность сравнения крайних групп и учет чувствительности пациента |37, 65]. Краткую форму шкалы оценки боли Глазго можно скачать на сайте http://www.gla.ac.uk/departments/painandwelfarere-searchgroup/downloadacutepamquestionnaire/.
Сходное средство было разработано для кошек, что стало важной вехой в распознавании боли у этих животных. В условиях клинических исследований сравнивались шкалы оценки боли, способные дифференцировать кошек, которым проводилось и не проводилось послеоперационное обезболивание, и шкалы, не обладающие такой способностью, а также шкалы, способные документально подтвердить различия между использовавшимися обезболивающими средствами [27, 96, 103].
На практике используется динамическая интерактивная визуальная аналоговая шкала (ВАШ) -простой и практичный способ для кошек. ВАШ представляет собой линию от 0 до 100 мм с ключевыми словами с обоих концов (рис. 2]. Проводящий оценку врач наблюдает за кошкой в спокойном состоянии, а затем проводит манипуляции с животным, пальпирует рану, если она имеется, и делает на линии отметку, если полагает, что кошка испытывает боль. Фармацевтическими компаниями была проведена значительная работа по оценке боли у кошек. Очень удобно использовать плакаты с фотографическим изображением элементов поведения, свидетелъствующих о боли у кошек; рекомендуется использовать их в сочетании с динамической интерактивной ВАШ для оценки боли.

Опиоиды
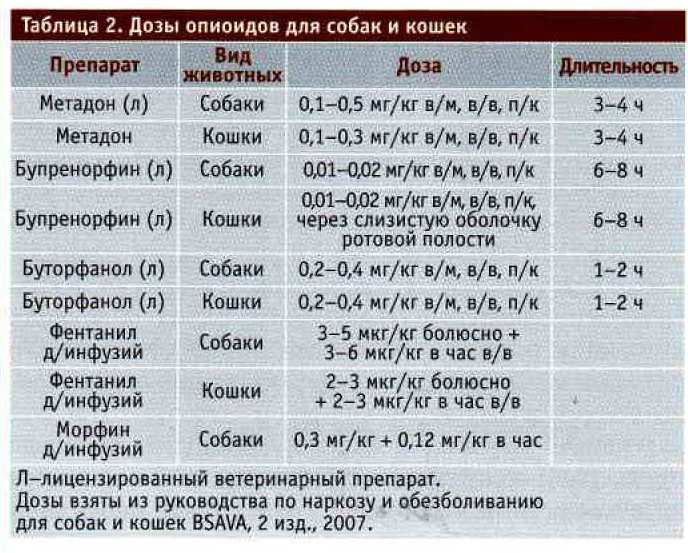
Опиоидные анальгетики (табл. 2} считаются основным средством ММО во время хирургических вмешательств и являются наиболее эффективными и часто используемыми препаратами для лечения болей от умеренной до сильной выраженности, причем при применении в рамках мультимодального режима их польза выше [39]. В ходе исследований опиоидных препаратов для ветеринарии были найдены средства с большей длительностью действия и меньшим числом побочных явлений. Использование таких препаратов, как метадон [51] или бупренорфин [96], позволяет избежать таких проблем, как малая продолжительность действия и высвобождение гистамина, как при использовании петидина, или рвотного эффекта, как при использовании метадона.
Как подробно описано в литературе, частичные агонисты мюопиоидных рецепторов, даже в максимальных дозах, неспособны создать такой же обезболивающий эффект, как чистые агонисты мюопиоидных рецепторов [35, 54]. Результатов ветеринарных клинических исследований, подтверждающих превосходство или меньшую эффективность частичных или полных агонистов мюопиоидных рецепторов, недостаточно; в медицинских исследованиях не было получено данных о превосходстве одного опиоида над другими, хотя для отдельных пациентов некоторые опиоиды оказываются эффективнее других [63].
Длительное действие и возможность введения разными способами относятся к преимуществам бупренорфина. Исследование с помощью оценки порога термической болевой реакции показало, что введение бупренорфина кошкам в дозе 0,02 мг/кг путем всасывания через слизистую оболочку ротовой полости настолько же эффективно, что и внутривенное (в/в) введение [81]. При применении меньшей дозы 0,01 мг/кг этого эффекта не обнаружено [27]. Это подчеркивает важность правильного подбора дозы. Robertson and others [81] комментируют, что при введении лекарств необходимо руководствоваться индивидуальной потребностью в связи с вариабельностью отклика у разных субъектов; эта особенность опиоидов в сочетании с разной чувствительностью к боли остается наиболее важной причиной вариабельности у человека [3].
В медицине, если при хронических болях повышение дозы не дает эффекта, можно попробовать заменить опиоидный препарат на другой [104], хотя для лечения острых болей такая практика не описана. По опыту авторов, периодическая замена опиоидных препаратов может оказаться эффективной при острых болях у собак и кошек; однако это не доказано формально.
Сообщается, что кривая зависимости ответа от дозы бупренорфина имеет колоколообразную форму, таким образом, возможно, что повышение дозы не повышает эффективность обезболивания, но может усугубить побочные явления [85]. При сравнении общепринятой дозы бупренорфина 0,02 мг/кг с дозой 0,04 мг/кг при оварио гистерэктомии собак не было обнаружено различий в частоте нежелательных явлений, а также повышения обезболивающего действия, что позволяет предположить эффект насыщения. Однако это могло быть обусловлено недостаточной чувствительностью использовавшихся методов, поэтому различие вес лее не исключено [99]. Среднее время до экстренного обезболивания в обеих группах составило 5 часов, что короче, чем обычная длительность действия бупренорфина - 6-8 часов, что подчеркивает важность оценки состояния животного через регулярные интервалы и обезболивания при необходимости.
Бупренорфин обладает высоким сродством к мю-опиоидным рецепторам, что может снизить обезболивающий эффект чистых агонистов мю-опиоидных рецепторов, назначаемых в последующем [96]. Собакам, которым проводилась овариоэктомия под изофлюрановым наркозом с инфузией суфентанила, для премедикации вводили бупренорфин либо физиологический раствор. Животным в группе бупренорфина требовалось в 2,5 раз больше суфентанила для поддержания гемодинамической стабильности, в связи с чем было- сделано заключение об отрицательном влиянии бупренорфина на антиноцицептивное действие суфентанила. Следовательно, введение бупренорфина следует прекратить за 6-8 часов до введения полных агонистов мю-опиоидных рецепторов [30].
Метадон, чистый агонист мю-опиоидных рецепторов, также действующий как неконкур ентный антагонист рецепторов NMDA [29], используется в ветеринарии с 1960-х гг. Лицензированные дозы для собак 0,5-1,0 мг/кг выше рекомендуемой дозы для человека ОД-0,5 мг/кг, что обеспечивает длительность действия 3-4 часа для собак и кошек [48]. При сравнении эффекта дозы 0,5-1,0 мг/кг, а именно снижения потребности собак в изофлютане, было сделано заключение, что эффект усиливается с повышением дозы, однако при этом отмечаются нежелательные явления в виде брадикардии, блокады предсердно-желудочкового узла третьей степени и остановки синусового узла у некоторых собак [11], которые зависят от дозы [64|.
Метадон в дозе 0,4 мг/кг характеризуется большим временем полувыведения при п/к введении по сравнению с в/в, возможно, из-за меньшей скорости всасывания. Исходя из результатов фармакоки-нетического моделирования, эти исследователи предлагают сначала вводить препарат в/в для создания соответствующих концентраций в плазме, а спустя 3 часа ввести его подкожно в дозе 0,4 мг/кг; в последующем подкожное введение повторяют дважды в сутки [38]. В этом исследовании побочным эффектом метадона у собак, не испытывавших боли, было скуление, которое не следует принимать за признак боли. Время полувыведения метадона варьирует от 1,7 до 4,3 часа [51]. Значение этого двояко. Во-первых, метадон хуже подходит для непрерывных инфузий, чем другие опиоиды, например фентанил, и, во-вторых, повторное введение должно проводиться по результатам оценки состояния животного, а не «по часам». До настоящего времени не проводилось совместных исследований фармакодинамики и фармакокинетики. В литературе описано удовлетворительное обезболивание кошек после овариогистерэктомии при применении метадона в дозе 0,6 мг/кг [83]; при этом антиноцицептивный эффект, оцениваемый путем измерения болевого порога при механическом раздражении, был очевиден после в/в введения (в дозе 0,3 мг/кг) и всасывания через слизистую оболочку ротовой полости (0,6 мг/кг). Общеизвестно, что буторфанол является слабым и кратковременно действующим анальгетиком [24, 80], его действие длится от 45 минут до 2 часов, возможно до 5 часов [18]. Это зависит от дозы, способа введения и модели антиноцицептивного действия. В литературе этот препарат всегда описывается как хороший анальгетик при висцеральных болях; однако этот эффект был отмечен в дозе 0,8 мг/кг п/к, что намного больше лицензированной дозы 0,2-0,3 мг/кг [89]. Буторфанол обеспечивает эквивалентное обезболивание в раннем послеоперационном периоде [111], хотя необходимы дальнейшие исследования для оценки эффективности этого средства в сравнении с другими лицензированными опиоидами.
Фентанил, чистый агонист мю-опиоидных рецепторов с быстрым и кратковременным действием, применяется для смешанной анестезии собак в дозе 30 мкг/кг в час [2]; сообщается о превосходном качестве анестезии в месте разреза кожи при болюсном в/в введении в дозе 2 мкг/кг [70]. Обезболивающий эффект однократного болюсного введения фентанила в дозе 10 мкг/кг показан на кошках без наркоза и характеризуется быстрым наступлением в течение 5 минут и длительностью действия 110 минут [82]; фентанил широко используется для обезболивания во время операций у этих животных [80]. Дозы, взятые из руководства по наркозу и обезболиванию собак и кошек BSAVA, приведены в табл. 2. Для собак и кошек автор использует дозы 1-2 мкг/кг в/в для обезболивания во время операции и непрерывную инфузию 5-10 мкг/кг в час.
Непрерывная инфузия опиоидов применяется как компонент сочетанного наркоза в целях уменьшения потребности в ингаляционных средствах для наркоза и, следовательно, снижения риска угнетения сердечной деятельности. Инфузий можно продолжать на протяжении периода восстановления от наркоза. Показано, что фентанил позволяет снизить дозу изофлюрана; он широко используется для обезболивания тяжелобольных пациентов как во время наркоза, так и в отделениях интенсивной терапии [78, 102]. При сочетании непрерывной инфузий фентанила в дозе 20 мкг/кг в час с изофлюраном или пропофолом для поддержания наркоза у травмированных кошек в группе пропофола-фентанила функция сердечно-сосудистой системы была стабильнее, хотя требовалась искусственная вентиляция с положительным давлением [59].
Сравнение морфина, вводимого путем инфузий [0,12 мг/кг в час) или инъекции в дозе 1 мг/кг в/м каждые 4 часа после абдоминальных операций показало равное обезболивающее действие при оценке по шкале Мельбурнского университета, хотя в группе, получавшей морфин в форме инфузий, его концентрации в плазме были ниже [60]. Когда антиноцицептивное действие у собак оценивали с помощью нитей фон Фрея, доза морфина 0,5 мг/кг в/в каждые 2 часа оказалась эффективнее, чем непрерывная инфузия в дозе 0,15 мг/кг в час [52]. До настоящего времени не проводилось исследований по оценке метадона для непрерывной инфузий.
Инфузия морфина-лидокаина-кетамина часто применяется в связи с ее удобством, однако оценки ее анальгетической эффективности не проводилось, кроме одного исследования, в котором было обнаружено уменьшение минимальной альвеолярной концентрации, сходное с наблюдаемым только при инфузий морфина" [67], что ставит под сомнение пользу такой комбинации.
В настоящее время предметом активных исследований являются простота применения и длительность эффекта ОПИОИДОБ. Разработана форма бупренорфина замедленного высвобождения, обеспечивающая обезболивание на протяжении 72 часов; эта форма была испытана на кошках после овариогисте-рэктомии [10]. Эффект однократного подкожного введения формы замедленного высвобождения по меньшей мере сравним с наблюдаемым при введении стандартной формы бупренорфина дважды в сутки. Опубликованы общие характеристики препарата (www.ema.europa.eu) для местной формы фентанила в виде раствора для собак.
Продукт прошел испытания в целях лицензирования, однако результатов исследований до настоящего времени не опубликовано. Можно ожидать, что анальгезия после однократного местного нанесения будет продолжаться до 4 суток; этот препарат показан собакам после крупных ортопедических и мягкотканных операций.
Нестероидные противовоспалительные препараты
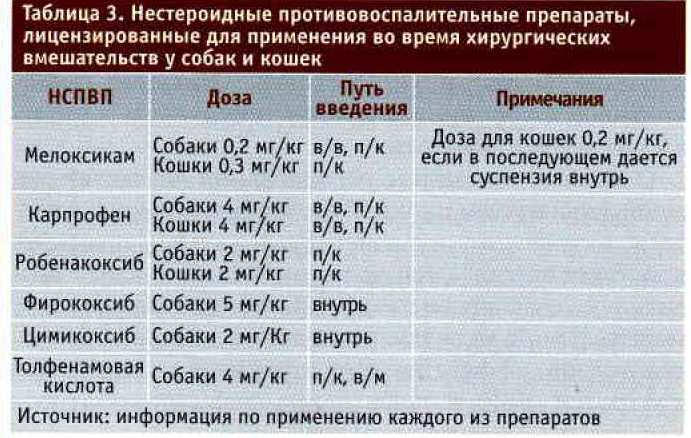
НСПВП - самые распространенные обезболивающие средства в ветеринарии [58] и один из лучших классов препаратов, применяющихся для лечения и профилактики послеоперационной боли [61]. Роль НСПВП при ММО очевидна, однако эти препараты описываются как «недостаточно эффективные в качестве единственного обезболивающего средства при сильных послеоперационных болях» [63]. В сочетании с опиоидами НСПВП обладали большей обезболивающей эффективностью в послеоперационный период и позволяли снизить дозу опиоидов для людей [63]; в ветеринарной литературе также опубликованы доказательства большей эффективности комбинации НСПВП и опиоидов [93, 97, 103]. НСПВП, лицензированные в Великобритании для применения во время хирургических вмешательств, представлены в табл. 3.
Избирательность НСПВП в отношении циклоок-сигеназы не связана с эффективностью, и ни одно из исследований не смогло доказать преимущества каких-либо конкретных НСПВП над другими. Характер нежелательных явлений сходен независимо от избирательности в отношении СОХ [5, 53, 73]; следовательно, выбор одного из перечисленных НСПВП на основании эффективности обезболивания или характера нежелательных явлений сложен.
Перед началом применения всегда следует учитывать противопоказания. Основными побочными явлениями НСПВП являются поражение желудочно-кишечного тракта и почек, последнее наиболее значимо во время хирургических вмешательств. Наркоз значительно снижает почечный кровоток -до 50 % по сравнению с исходным [25], и большинство случаев острой почечной недостаточности во время хирургических вмешательств у людей обус-
ловлено ишемией или интоксикацией [113]. Было проведено несколько исследований воздействия НСПВП на почки собак под наркозом, однако ни одно из них не смогло выявить чувствительные показатели острых почечных нарушений под действием НСПВП, особенно их влияние на почечный кровоток [53]. Описанные случаи нефропатий после применения НСПВП связаны либо с высокими дозами, либо с наличием других осложняющих факторов, таких как обезвоживание, недостаточное поддержание наркоза, шок или существующее почечное заболевание. Перед началом введения необходимо принять меры по устранению таких нарушений, как шок, обезвоживание, гипотензия, гиповолемия или кровоизлияние, а также тщательно контролировать функцию сердечно-сосудистой системы и проводить внутривенные инфузии для обеспечения достаточной перфузии жизненно важных органов [53].
Местные анестетики
Локальная/региональная анестезия подробно описана в руководстве по наркозу и обезболиванию BSAVA; описание каждой из техник выходит за рамки этого обзора, поэтому здесь представлена только новая информация. Преимущества локально-региональных методов хорошо описаны Сатроу and others [7]. «Местная анестезия препятствует передаче ноцицептивных импульсов и, следовательно, сводит к минимуму центральную сенсибилизацию, что снижает потребность в послеоперационном применении системных обезболивающих средств». Основным объектом настоящего иссле-
дования является разработка новых методов для ветеринарии, которые часто создаются путем модификации медицинских методов, описание новых подходов к хорошо известным техникам и улучшение их эффективности.
Основные принципы региональной анестезии перечислены в редакционной статье Британского Анестезиологического журнала: «Региональная анестезия действует всегда - при условии, что вы вводите правильную дозу правильного препарата в правильное место» [15]. К методам повышения точности и, следовательно, эффективности относится введение под контролем уЗИ и применение нейростимуляторов для поиска нервных стволов; описано применение обоих методов для блокады нервов тазовой конечности у собак [9, 94]. Альтернативы экстрадуральной анестезии включают блокаду бедренного и седалищного нерва. Такая блокада описана как безопасная и эффективная [112] и, кроме того, позволяет снизить потребность собак в опиоидах по сравнению с экстрадуральным введением морфина/бупивакаина [9]. Экстрадуралъная анестезия описана очень подробно [108].
Для анестезии дистальнее локтевого сустава применяется блокада лучевого, локтевого, срединного и мышечно-кожного нервов (RUMM) на уровне середины плеча [106). Добиться полной анестезии всех четырех нервов сложно, поэтому данная техника требует дополнительного исследования с использованием нейростимуляторов для поиска нервов и выполнения процедуры под контролем УЗИ в целях повышения эффективности. Описаны различные подходы к блокаде плечевого сплетения [8, 79]. К методам, прошедшим испытание в клинических условиях, относятся техника поиска нервов, позволяющая добиться анестезии при остеотомии плечевой кости у собак в 91 % случаев [26] и техника поиска нервов у кошек, способствующая снижению потребности в изофлюране и снижению послеоперационных болей [66].
Более новые техники включают интратекальный путь введения и блокаду поперечного пространства живота. Интратекальный (спинальный) метод не очень широко распространен в ветеринарии, однако гарантирует быстрое наступление действия по сравнению с экстрадуральным способом. Необходима дальнейшая работа для поиска оптимальных доз [87]. В медицине блокада поперечного пространства живота применяется для обезболивания брюшной стенки, способствует снижению потребности в опиоидах и повышает удовлетворенность пациентов [42]. Описано применение данного подхода для собак, хотя он требует клинической оценки [91].
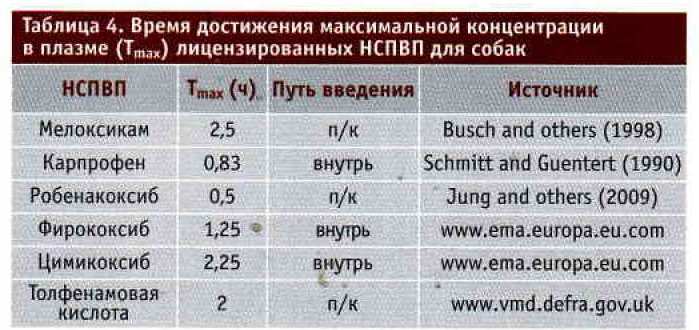
Установка катетеров в операционную рану
Возможные преимущества непрерывной инфилътрационной анестезии путем подачи раствора через катетер, введенный в рану (рис. 3), могут заинтересовать ветеринарных анестезиологов. В медицине накоплен значительный пласт доказательств, подтверждающих уменьшение болей, снижение потребности в опиоидах и сокращение срока госпитализации \33, 63]. у кошек, перенесших резекцию саркомы, установка катетеров в рану в целях обезболивания значительно сокращало время пребывания в стационаре [13]. Для подтверждения преимуществ этого метода необходимы дальнейшие ветеринарные исследования [1]. При резекции фибросарком и ампутации конечностей автор применяет буливакаин в дозе 1-2 мг/кг каждые 6-8 часов на протяжении 24 часов после операции.
Внутрисуставное обезболивание
Исследования с радиоактивно мечеными лигандами показали, что в воспаленных тканях суставов собак имеются участки связывания опиоидов [45j. Исследование, проведенное этими же авторами, не смогло показать эффекта внутрисуставного (в/с) введения морфина в сравнении с физиологическим раствором, поэтому было сделано заключение о необходимости дальнейших исследований для поиска дозы. В ходе двух предыдущих клинических исследований собак после оперативного лечения разрыва краниальной крестовидной связки было отмечено
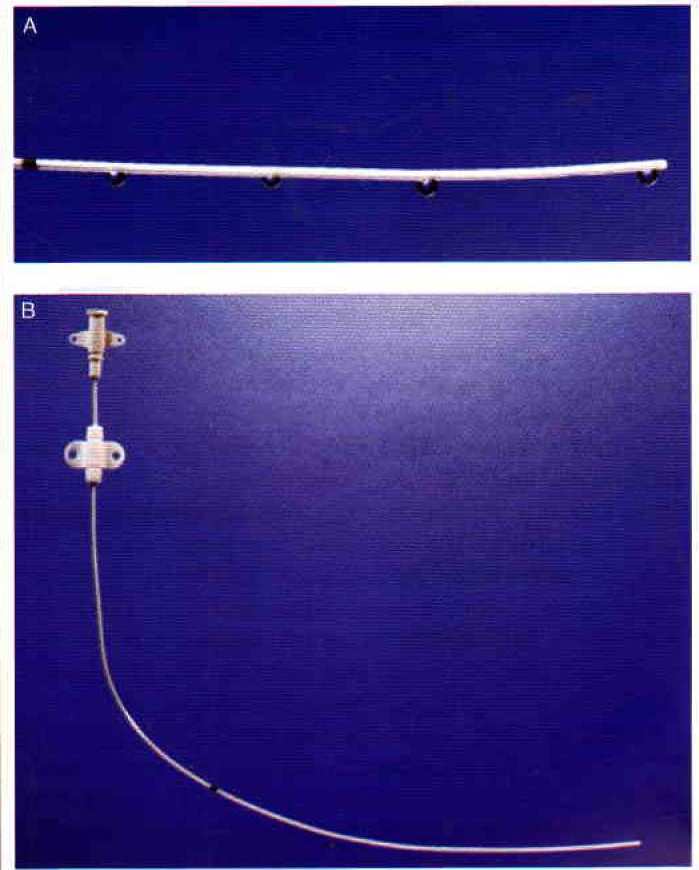
Рис. 3. Катетеры для инфильтрационной анестезии раны. (А) Поры в катетере. (В) Катетер для диффузии раствора в зоне операционной раны. Фото опубликованы с разрешения MILA International Inc.
благоприятное действие морфина в дозе 0,1 мг/кг Б/С [14, 86].
В одной работе описан благоприятный эффект в/с введения морфина, очевидный при измерении с помощью силоизмерительной пластины в качестве меры результата [34]. Результаты метаанализа, свидетельствующие о длительности обезболивающего эффекта до 24 часов после однократного введения морфина в коленный сустав человека [32, 43], были в последующем пересмотрены с учетом осложняющих оценку факторов [84], таких как степень воспаления, тип операции, исходная выраженность боли и интенсивность боли в ранний послеоперационный период.
Обезболивающее действие в/с введения бупивакаина описано у собак [34, 36, 86].
В связи с рядом случаев хондролиза у людей после артроскопии плечевого сустава и 72-часовой инфузии бупивакаина целесообразность внутрисуставного введения местных анестетиков была поставлена под сомнение [76|. Бупивакаин 0,5 % обладал большей хондротоксичностью, чем 0,25 %, и после 72-часовой инфузии 0,5 % бупивакаина наблюдались более значительные повреждения хондроцитов [17]. Влияние 0,125 % бупивакаина на хондроциты крупного рогатого скота не отличалось от влияния 0,9 % физиологического раствора. В редакторской статье Британского Анестезиологического журнала было сделано заключение, что при длительных инфузиях бупивакаина возможны нежелательные клинические явления, однако однократная инфузия бупивакаина в низкой концентрации представляется безопасной [114]. При исследовании in vitro токсическое действие мепивакаина на хондроциты лошади было меньше, чем у бупивакаина [74], а у собак после внутрисуставного введения мепивакаина отмечено притупление гемодинамической реакции на артросконическое вмешательство [19]. В связи с этими проблемами другие авторы предложили использовать альтернативные локально-региональные методы.
Лидокаин для инфузий
Лидокаин обладает различными свойствами; это самый известный местный анестетик в ветеринарии, относящийся к противоаритмическим средствам класса 1Ъ. Лидокаин для инфузии применяется в медицине для лечения острых и хронических болей, а дозы лидокаина ниже анестезирующих блокируют функцию активных или деполяризованных нейронов [72]. Такое действие наблюдается как в периферической нервной системе, так и в спинном мозге (16, 40]. Системное введение лидокаина блокирует распространение эктопических разрядов из места повреждения нейрона, а также в ганглиях дорсальных корешков [16]. Внутривенное введение лидокаина ослабляет боль и потребность в опиоидных препаратах после полостных операций у людей [63]. В ветеринарной анестезиологии этот препарат также применяется при острых болях у собак в тяжелом состоянии, так как обладает обезболивающими и противоаритмическими свойствами [20, 21]. Исследования на собаках кратко представлены в табл. 5. у кошек под изофлюрановым наркозом лидокаин вызывает тяжелое угнетение гемодинамики, поэтому применение этого препарата для кошек не рекомендуется [77]. Лидокаин в форме транедермального пластыря лицензирован в медицине при хронических болях и иногда применяется при острых болях у собак. В настоящее время проводятся клинические исследования пластыря бупивакаина II фазы; ожидается, что пластырь обеспечит анестезию в течение 3 суток [4].

Вспомогательные средства - кетамин
Кетамин, неконкурентный антагонист рецептора метил-О-аспартата (NMDA) на уровне спинного мозга, лучше всего известен в качестве средства для инъекционного наркоза, однако применяется также в качестве дополнительного обезболивающего средства. Антагонисты NMDA не действуют на поступление афферентных импульсов в дорсальный рог, однако препятствуют феномену «взвинчивания», тем самым превращая потенциальную ноцицептивную реакцию в нормальную [47]. Активация рецепторов NMDA глутаматом вносит вклад в центральную сенсибилизацию. К отличительным признакам центральной сенсибилизации относятся гипералгезия (усиленная реакция на болевые раздражители) и аллодиния (болезненная реакция на неболевые раздражители). Основная роль кетамина - противодействие гипералгезии, аллодинии и превентивное обезболивание, а не обезболивание само по себе [63]. Обезболивание кетамином не эквивалентно обезболиванию опиоидами [105]. Slingsby [95J рекомендует одновременное введение опиоидов. Такой подход практикуется в клинике автора для обезболивания во время хирургических вмешательств как у собак, так и у кошек; кетамин вводится в/в в дозе 0,5 мг/кг [20, 21] в сочетании с полными агонистами мю-опиоидных рецепторов (табл, 6),
Агонисты альфа-2-адренорецепторов
Агонисты альфа-2-адренорецепторов медетомидин и дексмедетомидин - мощные обезболивающие средства, действующие на уровне спинного мозга и выше. Их влияние на сердечно-сосудистую систему и антиноцицептивные эффекты хорошо описаны [69]. По данным исследования с измерением порога температурной болевой чувствительности, дексмедетомидин в сочетании с бупренорфином у кошек создавал более сильную седацию и обезболивание, чем каждый из препаратов по отдельности [98]. Данное сочетание анальгетиков удовлетворяет всем требованиям премедикации кошек перед наркозом.
Было проведено исследование на собаках, в котором дексмедетомидин в дозе 1 мг/кг сравнивался с морфином в дозе 0,1 мг/кг в час в форме непрерывной инфузии в течение 24 часов [107]. При этом среди клинических случаев не было отмечено значимых различий в выраженности седации, потребности в обезболивающих средствах во время операции или балльной оценке боли, у собак, которым требовалось дальнейшее обезболивание (морфин), в группе, получавшей дексмедетомидин в форме инфузии, балльная оценка боли была ниже, чем в группе, получавшей инфузию морфина, что подтверждает более эффективное обезболивание при сочетании данных препаратов [71, 98].
Дексмедетомидин может применяться не только в качестве обезболивающего средства, но и при комбинированном наркозе в целях снижения потребности в изофлюране у собак на 59 % в дозе 3 мкг/кг в час и на 18 % в дозе 0,5 мкг/кг в час [75]. Прочие препараты с благоприятным действием при острых болях у людей включают габапентин. Габапентин снижает послеоперационные боли и потребность в опиоидах, что повышает эффективность обезболивания в дополнение к НСПВП [63].
Прежде чем рекомендовать широкое применение на практике, необходимо провести дополнительные исследования на собаках и кошках.
ВЫВОДЫ
До настоящего времени большое внимание уделялось превентивной анальгезии; однако теперь новым горизонтом считается превентивная анальгезия с использованием мультимодальной техники.
По мере совершенствования методов оценки выраженности боли улучшаются наши возможности оценки боли у животных, а результаты исследования новых обезболивающих препаратов дают нам новые средства для облегчения боли.
Конфликт интересов
MAG работает в качестве консультанта в компании Eurovet Animal Health (комфортан) и читает лекции для Boehringer Ingelheim (мстакам), Novartis (онисор) и Elanco (дексдомитор/ домитор).



