Ж-Л. ПЕЛЛЕРЕН, К. ФУРНЕЛЬ, Л. ШАБАН
Аутоиммунные гемолитические анемии (АГА) - наиболее часто выявляемая разновидность аутоиммунных заболеваний у собак и кошек (Person J.M., Almosni R, Quintincolonna F, Boulouvis H.J., 1988). У собак первичная АГА возникает вследствие аутоиммунного заболевания. Часто обнаруживается и тяжело протекающая вторичная АГА нетравматической природы (Squires R., 1993).
АГА является одним из наиболее характерных классических примеров аутоиммунных заболеваний. Следовательно, в патогенезе АГА принимают участие аутоантитела (Miller G., Firth F.W., Swisher S.N., Young L.E., 1957). У человека идентифицирована специфичность антигенов-мишеней: имеются аутоантитела для антигена группы крови (Person J.M. etal., 1988).
АГА у человека была впервые открыта в 1945 году с помощью анти-глобулинового теста, получившего название метода Кумбса. Miller G. et al. (1957) впервые сообщили об АГА у собаки.
АГА была также выявлена у мышей, морских свинок, лошадей (Miller G. et al., 1957; Taylor FG.R., Cooke B.J., 1990), крупного рогатого скота (Dixon P.M. etal. 1978; FengerC.K., et al., 1992), овец, свиней, собак и кошек (Halliwel R.E.W., 1982).
ОПРЕДЕЛЕНИЕ
Под термином «анемия» подразумевают снижение концентрации гемоглобина в циркулирующей крови ниже 12 г на 100 мл у собак и ниже 8 г на 100 мл у кошек, что сопровождается уменьшением транспорта кислорода.
АГА определяют как приобретенный выраженный гемолиз, связан-
|
АНЕМИИ • Анемия - это не заболевание, а лишь синдром, этиология которого должна служить предметом исследований. • Термин «анемия» означает снижение концентрации циркулирующего в крови гемоглобина. Чаще всего при этом наблюдают уменьшение количества эритроцитов, однако это вовсе не обязательно. Нормальное содержание общего гемоглобина в крови собак колеблется в пределах 12-18 г на 100 мл крови. Мы говорим об анемии, если этот показатель падает ниже 12 г на 100 мл. У кошек порог концентрации гемоглобина в норме ниже-10 г/100 мл крови. • Обычно анемии подразделяют на регенеративные и арегенеративные. Это зависит от способности костного мозга поддерживать численность циркулирующих в периферической крови эритроцитов. • Регенеративная анемия Регенеративная анемия характеризуется появлением в периферической крови ретикулоцитов, дающих картину полихроматофилии, ассоциирующуюся в мазках с анизоцитозом. Регенеративные анемии, в свою очередь, подразделяются на регенеративные анемии вследствие кровопотери и анемии в результате гемолиза. • Гемолитическая анемия Гемолитические анемии характеризуются уменьшением продолжительности жизни эритроцитов. О наличии подобной анемии можно судить по продуктам деградации гемоглобина. Гемолиз может быть как внутри-, так и внесосудистым. По происхождению гемолитические анемии могут быть различными. Интракорпускулярные вызваны аномалией по типу интрансек собственно эритроцитов (как правило, имеют наследственный характер). Экстракорпускулярные: инфекционной или паразитарной природы (эрлихиоз собак, гемобартонеллез кошек, бабезиоз), вследствие интоксикации (например, отравление свинцом), нарушения иммунитета, в силу других причин (синдром ДВС - диссеминированной внутрисосудистой коагуляции). |
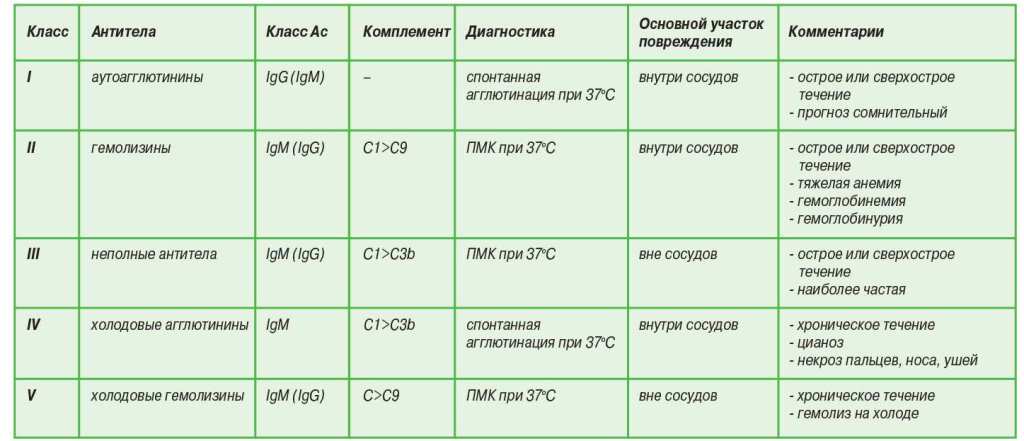
Таблица 1. Классификация АГА (ПМК = прямой метод Кумбса),
ный с присутствием иммуноглобулинов на поверхности эритроцитов и иногда в сыворотке крови, действие которых направлено по отношению к антигенным детерминантам мембраны эритроцитов больного (приложение 1).
АГА характеризуется двумя основными критериями:
1. диагностируется с помощью анализа крови;
2. аутоантитела выявляют с помощью прямого метода Кумбса.
Среди гемолитических анемий иммунной природы различают вторичные анемии, развивающиеся после аллогенной иммунизации, вследствие инфекционного процесса или медикаментозной сенсибилизации, а также - собственно АГА, sensu stricto (в строгом смысле слова). Аллоиммунизация очень редко встречается у собак и кошек.
КЛАССИФИКАЦИЯ
АГА классифицируют по иммунологическим и клиническим признакам
Критерии
Клиническая картина, результаты лабораторных исследований, патогенез, прогноз и лечение АГА во многом зависят от типа иммунопатологического процесса.
Иммунологическая классификация АГА основывается на классе антител (IgG или IgM) и их функциях -агглютинирующих или иногда гемолитических.
Классификация АГА включает пять основных классов (табл. 1). Холодовые агглютинины определяются как агглютинирующие антитела, выявляемые при температуре +4°С. Они всегда относятся к классу IgM.
Влияние на прогноз и терапию
АГА встречается чаще всего у собак и вызывается действием аутоиммунных IgG как вместе с комплементом, так и отдельно (Cotter S.M., 1992).
1. Если IgG экспрессированы на поверхности эритроцитов в ассоциации с комплементом или без его участия (класс I и III), то это заболевание в основном имеет идиопатическую природу с острым и транзиторным течением. Клиническая картина заболевания характеризуется последовательным развитием гемолиза, иногда протекающим тяжело и с ремиссиями. Эта первичная АГА, ассоциирующаяся с IgG, хорошо поддается лечению кортикостероидами и, как правило, не связана с вторичной АГА, возникающей вследствие каких-либо сопутствующих заболеваний. По данным Klag etcol. (1993), среди 42 собак, подверженных обследованию, 74% дали позитивную реакцию на IgG и негативную на комплемент. Подобные АГА в основном относят к классу III.
2. Если речь идет об антителах IgM (классы II, IV и V), то заболевание хуже поддается кортикостероидной терапии, чаще имеет вторичную природу (онкологическое, ин-
Таблица 2. Болезни собак и кошек, ассоциирующиеся сАГА(по Werner L).
* Болезни, вызванные пери- или интраэритроцитарными агентами, могут быть ответственными за развитие гемолитической анемии, опосредованной иммунитетом, без участия аутоантител, которые могут возникать вторично и осложняться развитием настоящей АГА.

фекционное или какое-либо другое аутоиммунное заболевание). Такие АГА могут быть выявлены непосредственно или опосредованно через присутствие СЗЬ и IgM при элюировании или смыве.
Прогноз АГА, ассоциирующейся с СЗЬ и IgM, более сомнительный по сравнению с IgG.
Распространенные иммунологические расстройства
У одного и того же пациента часто приходится наблюдать большое количество различных антител в соче-

тании с антиэритроцитарными аутоантителами. Особенно часто АГА собак сочетается с системной красной волчанкой (СКВ) или аутоиммунной тромбоцитопенией. В последнем случае речь идет о синдроме Эванса.
Синдром Эванса(Е. Robert, амер., 1951)[англ. Evans'syndrome]. Сии. syndrome de Ficher-Evans. Ассоциация аутоиммунного заболевания с тромбоцитопенической пурпурой. Редко встречается у человека, имеет сомнительный прогноз.
Иногда наблюдают АГА в ассоциации с аутоиммунным дерматозом, характеризующимся наличием депо IgG и комплемента на уровне дермоэпидермального сочленения (Hasegawa T. et al., 1990). Антиэритроцитарные аутоантитела являются фактором обширного иммунологического расстройства даже при отсутствии клинической картины заболевания.
Клиническая классификация
Иммунологическая классификация должна вступать в противоречие со строгой клинической, так как противопоставляет идиопатическую АГА вторичной АГА. Аутоиммунная гемолитическая анемия, характеризующаяся присутствием тепловых антител (IgG), соответствует «идиопатической», в то время как АГА, связанная с персистенцией Холодовых антител (IgM) - «вторичной».
Идиопатическая АГА
При первичной или так называемой идиоптической АГА не отмечают сопутствующих заболеваний. У собак частота АГА идиопатической природы составляет 60-75% случаев. У кошек это заболевания встречается редко, так как у них преобладает вторичная АГА по причине инфекционного заболевании, вызываемого вирусом лейкоза (FeLV) (Jackon M.L etal., 1969).
Вторичная АГА
В 25-40% случаев у собак и в 50-75% у кошек АГА ассоциируются с другими заболеваниями. АГА предшествует, сопровождает или следует за другим заболеванием, иногда протекающим без особых клинических симптомов (табл. 2). Прогноз и эффективность лечения зависит от первопричины АГА.
Вторичные АГА у кошек в основном ассоциируются с инфекцией FeLV или с гемобартонеллезом (Haemobartonella felis).
Частота обнаружения IgM на эритроцитах у кошек значительно превышает IgG, в то время как у собак преобладают аутоантитела класса IgG. Более высокое содержание антител класса IgM у кошки в сравнении с собаками объясняет преобладание реакции аутоагглютинации.
СИМПТОМЫ КЛИНИЧЕСКОЙ КАРТИНЫ ЗАБОЛЕВАНИЯ И РЕЗУЛЬТАТЫ ЛАБОРАТОРНОГО ИССЛЕДОВАНИЯ
У человека выявлена высокая положительная корреляция между признаками клинического, гематологического, иммунологического проявлений АГА (Stevart A.F., Feldman B.F., 1993).
Клинические симптомы
АГА проявляются в любом возрасте, однако наиболее часто их наблюдают с 2 до 7 лет. Также влияет время года (Klag A.R., 1992), поскольку 40% случаев АГА выявляют в маеиюне. У человека также обнаружено увеличение частоты заболевания АГА в весенний период (StevartA.F, Feldman B.F., 1993).
Пол и порода не являются факторами, предрасполагающими к данному заболеванию.
Начало заболевания может быть прогрессирующим или внезапным. Для АГА свойственно сочетание пяти патогномоничных симптомов:
1) упадок сил, вялость (86%)
2) бледность слизистых (76%)
3) гипертермия
4)тахипноэ (70%)
5) тахикардия (33%).
Тремя основными причинами обращения к ветеринарному врачу являются: коричневый цвет мочи, анорексия (90%) и упадок сил (Desnoyers M., 1992). Гепатомегалия и спленомегалия выявляются не всегда (25% случаев), аналогичную тенденцию отмечают и в отношении лимфаденопатии (Stewart A.R, Feldman B.F., 1993).
Также наблюдают прострацию и иногда летаргию. Желтушность, незначительна или отсутствует (50% случаев).
Петехии и экхимозы (кровоподтеки) наблюдают лишь в тех случаях, когда имеет место тромбоцитопения. По данным Klag A.R. et al. (1993) средняя или тяжелая тромбоцитопения наблюдалась у 28 собак из 42 (67%).
Интенсивность анемии может варьировать и зависит от 2 факторов:
1) степени гемолиза,
2) компенсаторной способности костного мозга.
Интенсивность анемии при первичной АГА по сравнению с вторичной более выражена.
Довольно редко при выявлении Холодовых агглютининов (IgM), чаще при идиопатической АГА анемия в целом выражена умеренно, с отдельными эпизодами усиления.
Цианоз и некроз концевых частей тела (уши, пальцы, хвост, нос) способные эволюционировать в гангрену, иногда с летальным исходом, являются наиболее патогно-моничными признаками при данном заболевании (Vandenbusshe P. etal., 1991).
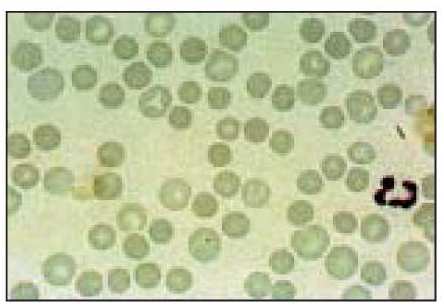
Рисунок. 1. Метод Кумбса: реакция агглютинации.
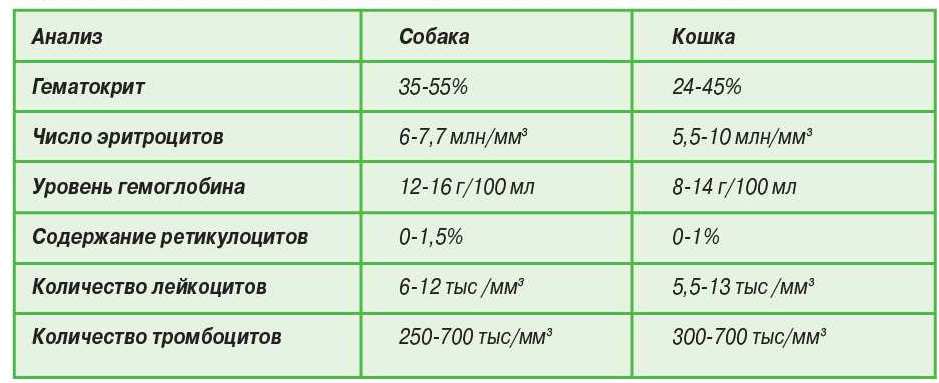
Таблица 3. Нормы общего биохимического анализа у домашних плотоядных (по Crespeau).

Приложение 3.
Все эти повреждения у собак и кошек связаны с нарушением кровообращения, порождаемым агглютинацией эритроцитов в периферических капиллярах, где температура тела значительно ниже таковой его висцеральной части.
Клинический анализ крови
При наличии АГА число эритроцитов падает ниже 5000000/мл. Гематокрит сильно снижен (до 8-10%), аналогичную картину наблюдают в отношении гемоглобина (до 4 г/100 мл). Отмечают нормоцитарную, нормохромную и иногда макроцитарную анемию (Jones D.R.E. etal., 1992, 1991, 1990).
Обращает на себя внимание наличие мелких окрашенных сфероцитов (фото 1), а также иногда отмечают нейтрофилию (Desnoyers M., 1992).
Порой мы констатируем фагоцитоз эритроцитов моноцитами. АГА у собак чаще имеет регенеративную форму (приложение 2). Общее количество ретикулоцитов варьирует от 20 до 60%. У 30% собак отмечают слабо выраженный ретикулоцитоз (1-3% ретикулоцитов), у 60% он умеренный или тяжелый (больше 3% ретикулоцитов). У собак были описаны слабо регенеративная и арегенеративная АГА (Jonas L.D., 1987). В настоящее время эти формы заболевания выявляются все чаще.
Биохимический анализ крови
У всех собак отмечают выраженную билирубинурию (коричневая окраска мочи) с уробилинурией, а также гипербилирубинемию (не коньюгированную). Желтушность присутствует приблизительно в 50% случаев. Возросшая гемоглобинемия иногда сопровождается гемоглобинурией, но симптом гемолиза внутри сосудов проявляется не так часто (10% из 42 собак) (Klag A.R. etal., 1993). При этом заметно снижение гаптоглобина и сывороточного железа, тогда как урикемия (мочевая кислота в крови) возрастает в 50% случаев. При развитии заболевания показатели варьируют, иногда изменения продолжительны или прерываются с последующими рецидивами.
МЕТОДЫ ИММУНОЛОГИЧЕСКОЙ ДИАГНОСТИКИ
Прямой тест Кумбса
Этот метод в диагностике АГА является приоритетным (Person etal., 1980).
Принцип
Тест Кумбса - это иммунологический метод, с помощью которого определяют наличие не агглютинирующих антител благодаря действию ксеногенной (от другого вида) антииммуноглобулиновой сыворотки, провоцирующей агглютинацию. С помощью одного лишь прямого теста Кумбса ставят диагноз на данное заболевание. В клинической практике этот метод используют для человека, собаки и кошки.
Принцип работы прямого теста Кумбса, или так называемого специального видового антиглобулинового теста, основан на эффекте сенсибилизации эритроцитов с помощью иммуноглобулина или комплемента, фиксирующихся на их мембране, либо за счет и одного и другого совместно (StewartA.R, 1993).
Механизм предлагаемого метода заключается в том, чтобы с помощью видоспецифических «анти-антител» или специфических антиглобулинов создать мостики между антителами, которые покрывают поверхность эритроцитов (рис. 1).
На первом этапе используют поливалентные антиглобулины, направленные против всех сывороточных глобулинов.
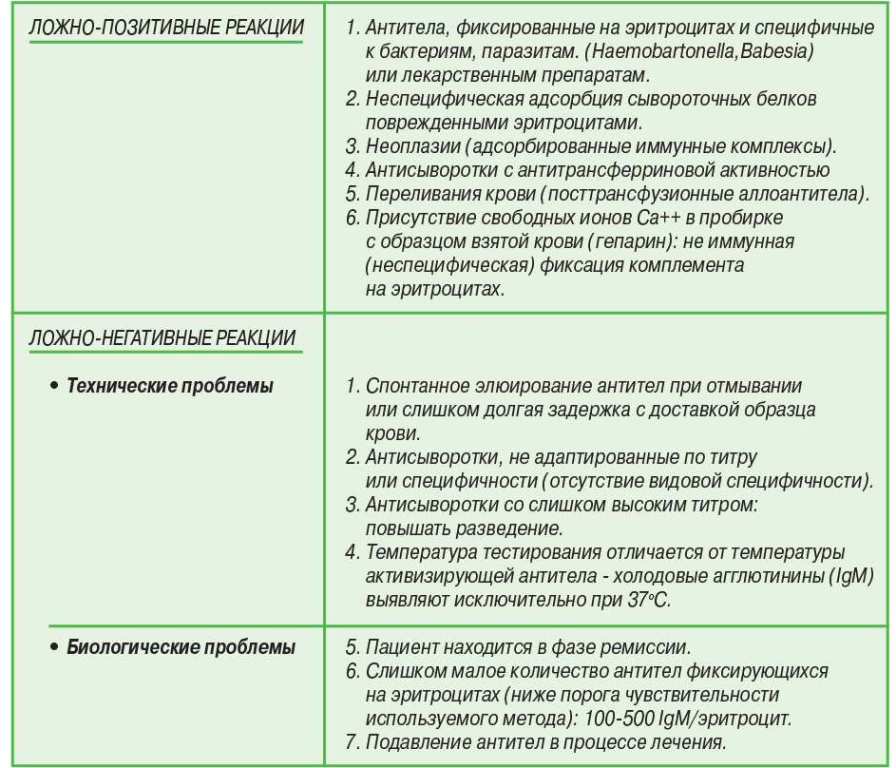
Таблща 4. Интерпретация результатов прямого метода Кумбса (по Cotter).
Классификация
Для человека разработаны следующие реактивы: анти-lgG, анти-IgM, анти-lgA и анти-СЗ.
Для собак в рутинной диагностике используют один поливалентный антиглобулин, иногда три антиглобулина: один поливалентный и два специфических - анти-lgG и анти-СЗ (Jones D.R.E., 1990).
• С помощью специфических реагентов установлено, что чаще всего эритроциты сенсибилизируются только одними IgG (АГА типа IgG), либо IgG в сочетании с комплементом (АГА смешанного типа), в частности с C3d, экспрессированным (присутствующим) на мембране эритроцитов.
• Иногда причиной сенсибилизации эритроцитов служит один лишь комплемент (АГА комплементного типа). Этот тип анемии связан исключительно с действием IgM, поскольку IgM при постановке теста Кумбса обычно элюируется спонтанно в процессе промывки. В данном случае после промывки при 37СС на поверхности эритроцитов остается только C3d.
IgM можно выявить через антикомплемент при использовании метода Кумбса, либо с помощью этого же метода, но проводимого на холоде, при котором элюирование IgM в процессе промывки не происходит. При этом мы говорим о Холодовых агглютининах IgM, когда при +4°С у собак можно наблюдать спонтанную агглютинацию.
• Антитела класса IgA встречаются крайне редко.
Каждый антиглобулин обладает видоспецифическими свойствами. Постановка реакции Кумбса с кошачьими эритроцитами означает необходимость своевременного приготовления или приобретения антиглобулинового реагента для этого вида животного. Наборы, предназначенные для проведения данного теста у человека или собаки, для кошек непригодны.
У домашних плотоядных АГА, выявляемые с Холодовыми антителами, встречаются гораздо реже, чем с тепловыми.
Техника выполнения
Кровь для анализа (приложение 3) необходимо брать с антикоагулянтом (цитрат или ЭДТА - этилендиаминотетрауксусная кислота). Крайне важно, чтобы в среде, находящейся пробирке, содержался агент, вызывающий хелатирование кальция. В образце крови он провоцирует неспецифическую фиксацию комплемента на эритроцитах в условиях in vitro и приводит к ложно позитивной реакции. Именно поэтому гепарин не используют в качестве антикоагулянта.
После тщательной отмывки (трех или пятикратное центрифугирование от 5 мин при 800д до 5 мин при 1500д) тестируемый образец суспензии ДОВОДЯТ до 2%-ой концентрации. Прямую реакцию Кумбса рекомендуется проводить как можно раньше с момента взятия материала, желательно в течение 2 часов. Образец крови следуетхранить при температуре 37°С. После инкубации в течение одного часа при 37°С с разными серийными разведениями трех антисывороток образец выдерживают в условиях комнатной температуры (1-1,5 часа). Результаты реакции учитывать визуально в лунках микроплашек, помещенных на зеркало Кана, либо с помощью микроскопа (х100).
Параллельно необходимо проводить негативные контроли:
1. 2%-ная суспензия эритроцитов больного в присутствии изотонического раствора NaCI с целью проверки способности тестируемых эритроцитов на спонтанную агглютинацию в отсутствие антиглобулинов. По данным Desnoyers M. (1992), аутоагглютинины отвечают за спонтанную аутоагглютинацию как при 37°С (класс I), так и при 4°С (класс IV). У кошек аутоагглютинация эритроцитов встречается часто (Shabre В., 1990). Разведение крови в эквивалентном объеме изотонического раствора NaCI позволяет исключить указанный артефакт за счет диссоциации эритроцитов, имеющих форму трубочек, не оказывая при этом негативного эффекта на настоящие аутоагглютинины (Squire R., 1993).
2. Смешивание 2%-ной суспензии эритроцитов здоровой собаки (контрольное животное) с видоспецифическим сывороточным антиглобулином позволяет проверить качество антисыворотки.
Если клинические симптомы указывают на АГА, опосредованную IgM, то клиницист может затребовать проведение обычной пробы Кумбса при 37°С, а также холодовой пробы Кумбса при 4°С, чтобы выявить антитела, активные на холоде (типы IV и V) (Vandenbussche P., et al., 1991).
Этот тест не приемлем для кошек. Дело в том, что у многих нормальных кошек есть неагглютинирующие антитела, которые становятся активными в условиях более низкой температуры и выявляются с помощью прямого теста Кумбса при 4°С. У данного вида животных следует использовать метод непрямой гемагглютинации при 4°С.

Обсуждение
Лабораторная диагностика АГА почти полностью основана на прямом методе Кумбса в сочетании с общим анализом крови. Интерпретация положительной реакции в тесте Кумбса не вызывает сложности.
• Если обнаруженные антитела относятся к классу IgG, то весьма вероятно, что выявленная анемия имеет аутоиммунное происхождение.
• Значимость выявления положительного результата в пробе Кумбса типа «lgG+комплемент» при АГА смешанного типа требует обсуждения, поскольку нет полной уверенности в том, что комплемент фиксируется на комплексе, образованном IgG с антигенами мембраны эритроцитов.
• Оказалось, что еще сложнее установить достоверность сенсибилизации эритроцитов при АГА, выявляемой с помощью позитивного теста Кумбса в постановке реакции на «чистый комплемент».
Возможно, часть тестов Кумбса типа «комплемент» соответствует временной фиксации комплексов антигенантитело, которые быстро элюируются с поверхности эритроцитов.
Дифференцируют АГА от истинного гипергемолиза по следующим признакам: повышенный ретикулоцитоз, неконьюгированная гипербилирубинемия и т.д. Иногда тест Кумбса дает ложно-позитивный или ложно-негативный результат (табл. 4). Это бывает довольно редко (примерно в 2% случаев), но негативная реакция на тест Кумбса может проявляться при истинной АГА, особенно если количество фиксированных иммуноглобулинов недостаточно (менее 500 на один эритроцит).
Клинические симптомы АГА во многом сходны с пироплазмозом, очень распространенным во Франции. Это требует от клинициста систематического проведения теста Кумбса в случае гемолитической анемии при отсутствии положительного ответа на классическое лечение, при заболевании животного пироплазмозом, даже если установлена персистенция пироплазм в крови, потому что это заболевание может одновременно сопровождаться АГА.
Элюирование
Если с помощью метода Кумбса можно определить, к какому классу относятся сенсибилизированные антитела, то элюирование позволяет определить их специфичность. Элюирование при высокой температуре с помощью эфира или кислоты позволяет собрать пул антител и протестировать их на панели с эритроцитами соответствующего вида с помощью непрямого метода Кумбса (Person J.M., 1988).
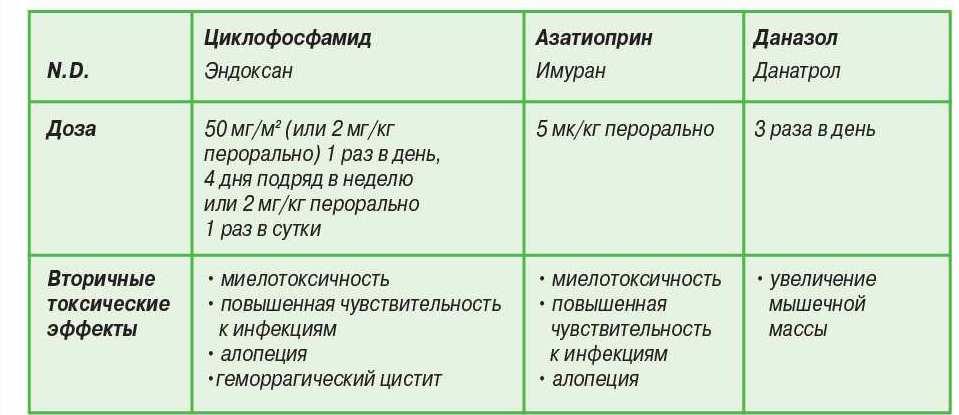
Таблица 5. Дозы используемых цитотоксических иммунодепрессивных препаратов и возможные токсические эффекты.
Это в основном проводят в гуманитарной медицине, где имеются панели с типированными эритроцитами.
У животных элюирование кислотой имеет особенное значение при подозрении на ложно-позитивную реакцию специфических антител к антигену, искусственно фиксированному на поверхности эритроцитов. Если элюат, полученный от эритроцитов собаки, подозреваемой на заболевание, не дает реакции агглютинации с пулом эритроцитов, полученных от собак с различными группами крови, то речь идет об АГА (Tsuchidaetal., 1991).
Непрямой метод Кумбса
Принцип его заключается в том, чтобы выявить наличие свободных аутоантител в сыворотке крови против эритроцитов.
Кровь больной собаки нужно собрать в чистую сухую пробирку и отцентрифугировать. Тестируемую сыворотку инкубируют в присутствии эритроцитов, трижды отмытых и полученных от здоровой собаки той же группы крови, что и больное животное. Уровень количества свободных аутоантител в сыворотке часто бывает очень низким, поскольку все присутствующие антитела плотно зафиксированы на поверхности эритроцитов. В 40% случаев количество свободных антител бывает недостаточным, чтобы получить позитивную реакцию в непрямом методе Кумбса (Stevart A.R, 1993).
МЕХАНИЗМЫ РАЗРУШЕНИЯ ЭРИТРОЦИТОВ
АГА входит в группу аутоиммунных заболеваний, для которых роль аутоантител в патогенезе продемонстрирована четко и убедительно.
Именно связывание аутоантител со специфическими антигенами на мембране эритроцитов ответственно за уменьшение продолжительности ихжизни, что опосредовано тремя цитотоксическими механизмами: 1) фагоцитоз; 2) прямой гемолиз при участии комплемента; 3) антителозависимая клеточная цитотоксичность.
Внесосудистый эритрофагоцитоз
В большинстве случаев наблюдается фагоцитоз эритроцитов макрофагами. Эритроциты, сенсибилизированные аутоантителами, разрушаются после опсонизации макрофагами селезенки, печени, в меньшей степени костного мозга. Билирубинемия, а также наличие в моче уробилина и билирубина подсказывают клиницисту о том, что происходит внесосудистый гемолиз (Chabre В., 1990).
Незначительные различия в патогенезе присутствуют между двумя «кладбищами эритроцитов» .
Внесосудистый эритрофагоцитоз может сочетаться с внутрисосудистым гемолизом.
Внутрисосудистый гемолиз, опосредованный комплементом
Деструкция эритроцитов в системе циркуляции довольно редкое явление (у 15% собак), которое наблюдается исключительно при острой гемолитической анемии, либо при острых осложнениях, развившихся при хроническом течении заболевания (классы II и V).
Это объясняется полной активацией комплемента по классическому пути от С, до Сд на поверхности одних и тех же эритроцитов. В результате происходит разрушение мембраны эритроцитов и высвобождение их составляющих (главным образом, гемоглобина) в циркулирующую кровь, что и приводит к гемоглобинемии и гемоглобинурии.
Это наблюдается только при фиксации аутоантител к комплементу с выраженным гемолитическим эффектом: роль в гемолизе в настоящее время четко установлена для IgG и IgM. Только эти формы аутоиммунного заболевания могут сопровождаться иктеричностью или субиктеричностью.
Цитотоксичность клеток, вызываемая антителами
К-клетки (клетки-киллеры или клетки-убийцы) имеют рецепторы к фрагменту Fc молекулы IgG, с помощью которых фиксируются на поверхности сенсибилизированных эритроцитов и вызывают их гибель посредством прямого цитотоксического воздействия.
Недавно точно установлена, но еще не совсем точно определена роль этого третьего механизма в развитии АГА.
ПРОГНОЗ
Как и при остальных аутоиммунных заболеваниях, степень аутоиммунных нарушений не всегда прямо пропорциональна тяжести проявления процесса.
Краткосрочный прогноз
Краткосрочный прогноз неблагоприятный лишь в 15-35% случаев. Клиническое улучшение после адекватной терапии наблюдается, по данным разных авторов, у 65-85% пациентов.
Увеличение гематокрита и ретикулоцитоза на фоне снижения сфероцитоза - положительные прогностические критерии.
Смертность собак значительно повышается при следующих обстоятельствах: слабая регенерация (умеренный или недостаточный ретикулоцитоз), низкий гематокрит (ниже 15%), концентрация билирубина в крови выше 100 мг/л.
Долгосрочный прогноз
Долгосрочный прогноз менее благоприятен в плане возможных осложнений. Обычно приходится довольствоваться тем, что выздоровление достигается лишь в 30-50% случаев.
Прогноз при вторичной АГА зависит главным образом от сопутствующего заболевания и его возможных осложнений.
Чаще всего наблюдается легочная тромбоэмболия и диссеминированная внутрисосудистая коагуляция (Cotter S.M., 1992). В редких случаях отмечают осложнения в виде лимфаденита, эндокардита, гепатита или гломерулонефрита, которые могут привести к летальному исходу (Stewart A.F., Feldman B.F, 1993).
При заболевании класса III прогноз чаще всего благоприятный. У кошек прогноз сдержанный, поскольку заболевание нередко ассоциируется с инфекцией, вызванной тем или иным ретровирусом (вирус кошачьей лейкемии, FeLV; вирус кошачьего иммунодефицита, VIF) (ChabreB., 1990).
Более осторожный прогноз при заболеваниях классов II и V, сопровождающихся внутрисосудистым гемолизом.
Прогноз сомнительный при заболеваниях, относящихся к классам I и IV и сопровождающихся аутоагглютинацией (Hagedorn J.E., 1988). Они чаще остальных заканчиваются летальным исходом.
По данным Klag et col. (1992, 1993) общий уровень смертности составляет около 29%.
В любом случае прогноз должен быть всегда сдержанным и зависеть от адекватности фармакологической коррекции состояния.
ЛЕЧЕНИЕ
Терапия АГА может осуществляться различным образом. Наиболее общий подход лечения основан на устранении иммунологической реакции путем назначения иммуно-депрессантов, которые подавляют образование аутоантител и активность макрофагов, ответственных за эритрофагоцитоз.
Иммунодепрессанты
Кортикостероиды - главная составляющая терапии. Они применяются как в виде монотерапии, так и в ассоциации с даназолом, циклофосфамидом или азатиоприном (Cotter S.M., 1992; Squires R., 1993).
Кортикостероиды
В высокой терапевтической дозе и при длительном применении кортикостероиды являются основными препаратами, обеспечивающими эффект иммунодепрессии. С точки зрения клинициста преднизон (Cortancyl N.D. per os), преднизолон, метилпреднизолон (гемисукцинат метилпреднизолона: Solumedrol N.D., в/в), назначаемые в ударных дозах от 2 до 4 мг/кг через каждые 12 часов, дают наилучший результат. Также можно использовать дексаметазон или бетаметазон в дозах 0,3-0.9 мг/кг в сутки (Stewart A.F., Feldman B.F, 1993).
Если кортикостероидная терапия эффективна при АГА с тепловыми аутоантителами (IgG) в 80-90% случаев, то при АГА с Холодовыми аутоантителами (IgM) её результативность неоднозначна. Тем не менее, полученные данные следует оценивать самым тщательным образом. Если кортикостероидная терапия неэффективна, необходимо прибегнуть к цитотоксической химиотерапии.
• Ударная кортикостероидная терапия должна быть начата как можно раньше с момента подтверждения диагноза на АГА с помощью прямого метода Кумбса. Лечение не должно быть длительным: продолжительность варьирует в среднем от трех до восьми недель. Больший курс кортикостероидной терапии имеет незначительные преимущества, но сопряжен с риском тяжелых осложнений (ятрогенный синдром Кушинга).
• При поддерживающей терапии кортикостероиды назначают через день в дозах, равных половине, четверти или одной восьмой от ударной. Постепенную отмену препаратов осуществляют в течение двух-четырех месяцев после клинической ремиссии. Некоторым животным отменяют кортикостероиды полностью. Других продолжают лечить с применением низких доз в течение всей жизни для исключения рецидивов (Squires R., 1993).
У собак с идиопатической АГА (IgG) тест Кумбса остается положительным на всем протяжении заболевания, в том числе во время кортикостероидной терапии и клинической ремиссии. Когда же в прямом методе Кумбса реакция негативная, то рецидив заболевания бывает довольно редко. Речь идет об очень благоприятном прогностическом критерии (Slappendel R.J., 1979).
У кошек кортикостероидную терапию сочетают с назначением антибиотиков тетрациклинового ряда, если при гематологическом исследовании выявлен гемобартенеллез (Haemobartenella felis), либо для профилактики бактериальных осложнений на фоне иммуносупрессии.
Кортикостероидную терапию у кошек не следует проводить длительно, особенно при инфекции, вызванной FeLV. Иммунодепрессивное действие кортикостероидов может усилить и без того выраженный иммунодепрессивный эффект вируса. У кошек с латентной вирусной инфекцией кортикостероидная терапия может обострить патологию и вызвать виремию.
Если в первые 48-72 часов после начала кортикостероидной терапии не удается достигнуть стабилизации или улучшения показателя гематокрита, то терапию следует продолжить. Заметное увеличение гематокрита может произойти через 3-9 дней после начала терапии. Если улучшения не произошло и по истечении 9 дней, то следует использовать более мощные иммуно-депрессивные препараты.
Мощные иммунодепрессанты
Циклофосфамид и азатиоприн два цитотоксических препарата (цитостатики), являющиеся более мощными, чем кортикостероиды иммунодепрессантами (табл. 5). Они подавляют выработку антител В-лимфоцитами (Squires R., 1993).
Применять эти препараты следует лишь в самых тяжелых случаях заболевания АГА: пациентам с аутоагглютинацией (классы I и IV) или с внутрисосудистым гемолизом (классы II и V) (Hagedorn J.E., 1988). В тяжелых случаях требуются меры энергичного терапевтического воздействия. Обязательно следует информировать владельцев животных о побочных эффектах препаратов.
Циклоспорин (10 мг/кг, в/м, затем перорально в течение 10 дней) успешно применяют для лечения сложных рецидивирующих случаев АГА, не поддающихся классической кортикостероидной терапии (Jenkins TS. et al., 1986; Preloud P., Daffos L, 1989). Пациентам с аутоагглютинацией (классы I и IV) для профилактики рецидивов и достижения ремиссии требуется сочетанная терапия (кортикостероиды + цитостатики). Однако для лучшего понимания того, насколько такое сочетание эффективно при терапии АГА, требуются более масштабные испытания.
Даназол
Даназол (производное этистерона), синтетический гормон группы андрогенов, все чаще и чаще применяют для лечения аутоиммунных заболеваний (Stewart A.F., 1945). Даназол снижает продукцию IgG, a так же количество IgG и комплемента, фиксированных на клетках (HollowayS.A. etal., 1990).
Основной механизм действия даназола заключается в ингибировании активации комплемента и в подавлении фиксации комплемента на клеточных мембранах (Bloom J.C., 1989). Даназол модулирует соотношение Т-хелперов и Т-супрессоров, которое нарушается при аутоиммунной тромбоцитопении (Bloom J.C., 1989). Он также может снижать количество рецепторов к Fc фрагменту иммуноглобулинов, находящихся на поверхности макрофагов (SchreiberA.D., 1987).
Терапевтическая доза для собак составляет 5 мг/кг, 3 раза в день перорально (Stewart A.R, Feldman B.F., 1993). Действие даназола (Danocrine N.D., Danatrol M.D.) нарастает медленно в течение одной или трех недель и проявляется в улучшении гематологических показателей (Bloom J.C., 1989; Schreiber A.D., 1987). Рекомендуется сочетать даназол с каким-либо кортико-стероидом (Stewart A.F., Feldman B.F., 1993). Когда состояние пациента стабилизируется, дозы корти-костероидов уменьшают, а лечение даназолом продолжают в течение двух-трех месяцев (Schreiber A.D., 1987). Даназол может вызвать заметное увеличение мышечной массы, если его использовать более полугода.
Спленэктомия
Цель спленэктомии заключается в удалении селезенки, которая является основным органом деструкции эритроцитов в случае АГА, связанной с IgG. Она также является главным органом лимфоидной системы, продуцирующим циркулирующие антитела, в конкретном случае аутоантитела. Успешно применяемая в гуманитарной медицине, эта операция, вероятно, не может быть столь же благоприятной для собаки и кошки (Feldman B.F. et al., 1985). Она совершенно бесполезна при АГА, связанной с IgM, где деструкция эритроцитов в основном происходит в печени. Более того, выполнение данной операции может вызвать обострение латентного течения бабезиоза или гемобартонеллеза. Таким образом, мы предлагаем рассматривать спленэктомию лишь как крайний вариант (Feldman В.Fetal., 1985).
Переливание крови
Гемотрансфузия в основном противопоказана из-за возможности возникновения гемолиза. Переливаемые эритроциты быстро покрываются аутоантителами, что приводит к их массовому разрыву, и, следовательно, усугублению криза гемолиза. С другой стороны, гемотрансфузия снижает нормальный гемопоэз костного мозга. Поэтому её следует назначать по следующим показаниям: гемолитический криз, гематокрит ниже 10% или нарушение дыхания.
На практике показанием для гемотрансфузии считается падение числа эритроцитов ниже 2x106 /мл у собак и 1,5x106/мл у кошек. Очень кратковременное улучшение отмечают при внутривенном введении кортикостероидов. Плазмаферез дает положительные результаты у человека, но у животных его применение осложняется малой доступностью приборной техники для собаки кошек (Matus R.E. etal., 1985).
Адъювантная терапия
Как и при всех анемиях используют адъювантную терапию: сульфат железа из расчета 60-300 мг в сутки (Squires R., 1993), витамин В12, спокойная обстановка, тепло, а затем внутривенная инфузия, иногда принудительное дыхание. Особенно важно, чтобы пациентов с холодовыми агглютининами оберегали от воздействия слишком низких температур. Профилактика тромбоэмболии и ДВС синдромау собак группы риска (повышенный уровень общего билирубина, состояние после гемотрансфузии) заключается в раннем введении антикоагулянтов: 100 ЕД/кг гепарина п/к каждые 6 часов на протяжении периода обострения (Klein M.K. et al., 1989).
Наблюдение за пациентами
Это имеет большое значение. Контроль над состоянием пациентов можно осуществлять с помощью теста Кумбса: через два месяца с момента вхождения больного в острую фазу течения заболевания, затем через каждые 2-3 месяца при переходе в хроническое течение. Если критерии клинической и гематологической оценки свидетельствуют о норме, тест Кумбса дает отрицательную реакцию, можно считать, что собака или кошка выздоровели. Однако трудно говорить об истинном выздоровлении или простой ремиссии.
В этом случае следует быть крайне осторожным, поскольку с вероятностью 50% возможен любой из вышеуказанных вариантов.
Для выяснения истинной обстановки необходимо продолжать контроль за состоянием животного, систематически проводить анализы крови (например, один раз в месяц в течение полугода, а потом один раз в три месяца) и при малейшей угрозе рецидива возобновлять кортикостероидную терапию. Как правило, этого бывает достаточно для нормализации клинического состояния. Минимальная доза кортикостероидов (0,05-1 мг/кг в день) через день способствует восстановлению показателей крови до физиологической нормы. При хроническом или рецидивирующем течении АГА рекомендуется перманентное назначение кортикостероидов по мере возможности в минимальной терапевтической дозе.
ЗАКЛЮЧЕНИЕ
Когда клиническая картина достаточно показательна, то с помощью только одного прямого метода Кумбса можно поставить диагноз на АГА. Но это относится только к позитивной реакции теста Кумбса в присутствии IgG (как вместе с комплементом, так и без него). В целом, позитивные реакции с одним лишь комплементом часто встречаются у собак и редко ассоциируются с выраженным гемолизом. Если поставлен предварительный диагноз, то необходимо проведение дополнительных исследований. Как и при всех аутоиммунных заболеваниях, неспецифические нарушения в иммунной системе могут быть вызваны самыми разными причинами.
И, наконец, все аутоиммунные заболевания имеют сходства, причем каждое представляет группу нарушений, которые в той или иной степени наслаиваются друг на друга. Нередко, можно наблюдать одновременное или последовательное проявление АГА и системной красной волчанки, и АГА и ревматоидного полиартрита, либо АГА и аутоиммунной тромбоцитопении. Если с помощью постановки иммунологического диагноза выявлено наличие одного из этих аутоиммунных заболеваний, то нужно обязательно искать и другие даже при отсутствии характерных клинических симптомов. При ассоциации АГА с СКВ или тромбоцитопенией у собаки, или с инфекцией FeLV у кошки прогноз более сомнительный по сравнению с изолированной идиопатической АГА.
журнал "Ветеринар" № 2003



