Кузнецов Ю. Е., Никонова Э. Б., Новиков Д. Д.
ФГБОУ ВПО «Санкт-Петербургская государственная академия ветеринарной медицины» Адрес: 198280, Россия, Санкт-Петербург, ул. Черниговская, 5
Введение
Широкий спектр фармакологического действия 2-метил-6-метил-3 оксипиридина сукцината подтвержден при лечении животных при токсикозах, стрессовых ситуациях при перевозке и т. д. [5, 7, 8]. У животных, получавших 2-метил-6-метил-3 оксипиридина сукцинат, заметно увеличивался энергетический потенциал, ярко проявлялись породные признаки собак, улучшалась управляемость ими [3, 4].
Фирмой ООО «НВЦ Агроветзащита» разработан и представлен для изучения препарат Эмидонол 10 % в форме рас-твора для инъекций, который содержит в 1 мл в качестве действующего вещества 2-метил-6-метил-3 оксипиридина сукцинат — 100 мг/мл.
Целью наших исследований явилось изучение местно-раздражающих и аллергенных свойств препарата.
Материалы и методы
Кожно-резорбтивное действие препарата изучалось в повторном опыте на 20 белых мышах. Животных помещали в специальные домики, а их хвосты на 2/3 длины погружали в пробирки с чистым препаратом. Экспозиция 2 часа на протяжении 14 дней. Контрольные животные находились в тех же условиях, а их хвосты погружались в воду.
При изучении способности препарата проникать через кожу использовались те же показатели, что и в предыдущем опыте.
Раздражающее и аллергическое действие препарата изучалось на 5 кроликах породы «Шиншилла», согласно «Руководству по экспериментальному (доклиническому) изучению новых фармакологических веществ», 2007 [6].
В первой серии опыта проведено тестирование препарата в разных концентрациях. Препарат наносился на выстриженные (3Х3) участки боковой поверхности кожи кроликов 5 раз в неделю на протяжении 2 недель. Ежедневная экспозиция - 4 часа, после чего препарат смывали водой. Реакцию кожи оценивали по шкале Суворова [2, 6].
Этот опыт позволяет выявить опасность развития неаллергического контактного дерматита и одновременно подобрать концентрацию, не обладающую раздражающим действием.
Во второй серии препарат в «рабочей» дозе наносился на левый бок кролика, где выстригался участок кожи размером 4x4 см. Экспозиция 4 часа, 5 раз в неделю, на протяжении 20 дней.
Первое тестирование по шкале оценки кожных проб проводилось через 10 дней. При этом выстригали кожу на противоположном боку кролика и наносили препарат в той же дозе. Реакцию кожи анализировали на 24, 48 и 72 часа после смывания продукта. При отрицательном результате опыт продолжили и довели число аппликаций до 20, после чего проводили повторное тестирование.
Для количественной оценки сенсибилизации к препарату использовали иммунологический метод по выявлению реакции клеток крови на аллерген in vitro - реакцию дегрануляции тучных клеток (РНДТК) и реакцию гистаминового шока.
Исследование раздражающего действия препарата на слизистые оболочки глаз про-водили на кроликах. Препарат в количестве 3 капель вносился в конъюнктивальный мешок правого глаза трем кроликам. Левые глаза кроликов служили контролем. Наблюдение за состоянием животных проводилось в течение 2 недель. Оценку раздражающего действия проводили согласно рекомендаций [6], учитывая изменение кровенаполнения конъюнктивы, состояние роговицы и радужной оболочки, количество выделений из глаз.
Результаты и обсуждения исследований
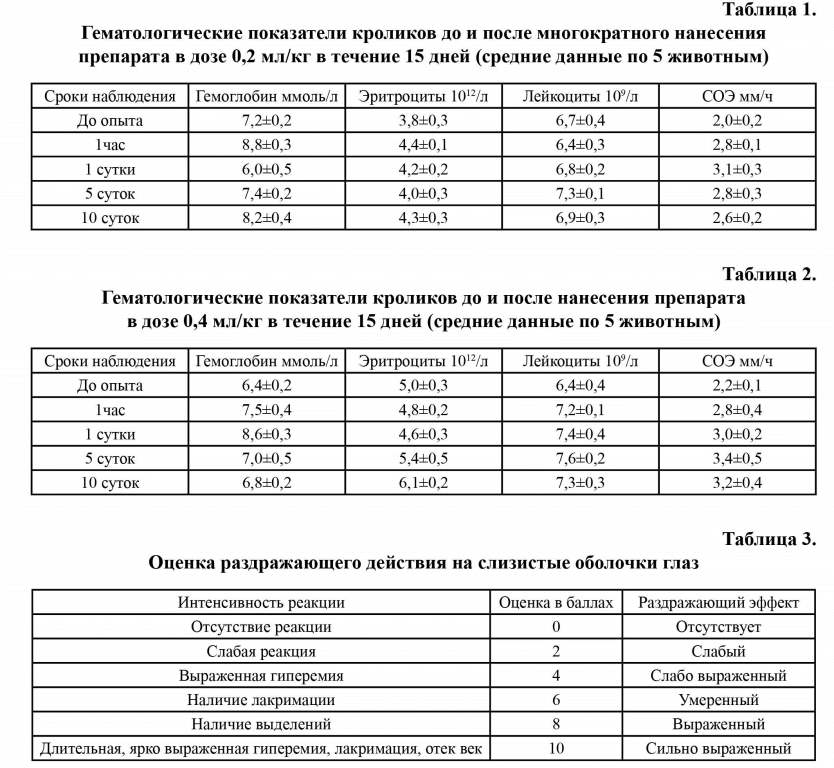
Результаты исследования раздражающих свойств препарата показали, что нанесение Эмидонола 10 % на кожу в дозах 0,2-0,4 мл/кг ежедневно в течение 15 суток не вызывало у кроликов изменений кожного покрова. Не отмечено покраснения кожи, утолщения кожной складки и выпадения подстриженной шерсти и шерсти, граничащей с выстрижен-ными участками.
При пальпации выстриженных участков кожи не наблюдали болезненной реакции у животных. Данные гематологических показателей свидетельствуют, что нанесение препарата на выстриженные участки кожи кроликов в дозах 0,2 и 0,4 мл в течение 15 суток существенно не изменяли картину крови животных (таблица 1 и 2).
Опыт по изучению раздражающих свойств препарата на слизистые оболочки глаз провели на 5 кроликах.
Раздражающее действие препарата на слизистые оболочки глаз определяли по «глазной пробе» [2, 6]. В конъюнктивальный мешок левого глаза 5 кроликам закапывали 1-2 капли препарата, а в конъюнктивальный мешок правого - 1-2 капли воды. За животными вели наблюдение на протяжении 15 суток. Оценку раздражающего действия проводили через 1, 2, 3, 4 и 24 часа, 3-7 и 15 суток визуально по изменению кровенаполнения конъюнктивы, наличию лакримации и состоянию роговицы по 10 бальной системе согласно таблице 3.
Через 1 час после введения препарата у всех подопытных животных наблюдали слезотечение и выраженную гиперемию конъюнктивы с оценкой 4 балла. Через 2, 3 и 4 часа конъюнктива оставалась слабовыраженной в той же степени - 4 балла.
Спустя 24 часа у всех кроликов на слизи-стой глаз имело место наличие лакримации и отека век (раздражающий эффект - умеренный). На 2 сутки отмечали ярко выраженную гиперемию и лакримацию (раздражающий эффект - умеренный). На 4-е сутки признаки раздражения слизистой глаз постепенно исчезали. На 7 сутки видимых изменений на слизистой оболочки глаз не наблюдали. Таким образом было установлено, что испытуемый препарат обладает умеренным раздражающим эффектом на слизистые оболочки глаз в течение первых 2 суток.
Изучение аллергизирующего действия Эмидонола 10 %
При введении подопытным животным гистамина наблюдалась следующая реакция: возбуждение, частая дефекация, мочеиспускание, учащенное дыхание, судороги и смерть. Критерием оценки служило время от момента введения гистамина до момента бокового положения животных. Время наступления гистаминового шока у подопытных и контрольных животных находилось в близких пределах (Р > 0,05). Не было отмечено укорочения периода наступления гистаминового шока при введении Эмидонола 10 % как в терапевтической, так и в три раза увеличенной терапевтической дозах (табл. 4). Препарат в указанных дозах не потенцировал эффекта гистамина и, следовательно, не проявлял аллергизирующих свойств.
У подопытных морских свинок характер протекания гистаминового шока не отличался от такового у контрольных животных.
В своих исследованиях мы применили также тест непрямой реакции дегрануляции тучных клеток крыс (РНДТК).
Опыты по изучению аллергенных свойств по тесту «непрямой реакции дегрануляции тучных клеток» показали, что при подкожном введении препарата в терапев-тической и в три раза увеличенной дозах на первые сутки после введения процент дегранулированных клеток не превышал десяти (табл. 5). На 5, 10 и 15 сутки после введения препарата процент дегранулированных клеток находился в пределах 4,8±0,2 - 2,8±0,30. Таким образом, наибольший процент дегранулированных клеток наблюдался на первые сутки после введения препарата Эмидонол 10 % в дозах 0,2 и 0,6 мл/кг, но и в эти сроки по количеству дегранулированных клеток реакция считается отрицательной.
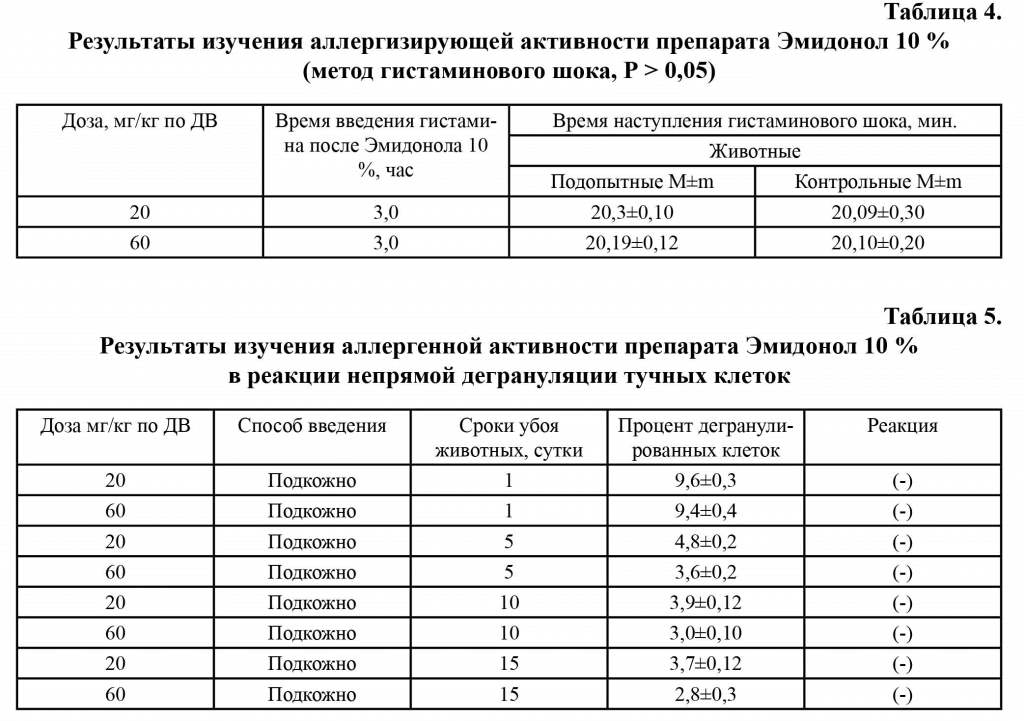
Таким образом, с использованием двух высокочувствительных тестов для определения аллергизирующей активности препарата Эмидонол 10 % - «гистаминового шока» и РНДТК - мы установили, что препарат при подкожном пути введения в терапевтической и в три раза увеличенной дозах не потенцирует влияние гистамина и не вызывает дегрануляции тучных клеток крыс, выходящие за пределы нормы.
Заключение
Препарат не обладает местно-раздражающими свойствами и не вызывает аллергической реакции у животных в испытанных дозах и будет рекомендован к регистрации.
Список литературы
1. Антрошенко, О. Н. Поиск фармакологических корректоров работоспособности в постгипоксический период в ряду производных 3-оксипиридина: автореферат дисс. ... канд. мед. наук О. Н. Антрошенко. -М., 1997.
2. Беленький, М. Л. Элементы количественной оценки фармакологического эффекта / М. Л. Беленький. — Изд. 2-е, переработ, и доп. - Л. : Мед. литература, 1963.-С. 152,81-101.
3. Бурлакова, Е. Б. Свободнорадикальное окисление липидов в норме и патологии / Е. Б. Бурлакова. — М., 1976.
4. Бурлакова, Е. Б. Биоантиоксиданты вчера, сегодня, завтра : Сборник трудов V Международной конференции Биантиоксидант / Е. Б. Бурлакова. - М., 1998.
5. Дюмаев, К. М. Антиоксиданты в профилактике и терапии патологий ЦНС / К. М. Дюмаев, Т. А. Воронина, Л. Д. Смирнов. -М., 1995.-272 С.
6. Хабриев, Р. У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / Р. У. Хабриев. - Изд. 2-е. - М., 2007. - С. 41-54.
7. Sherding, R. G. Diseases of the Small Bowel. Textbook of Veterinary Internal Medicine / R. G. Sherding. - 1983.
8. Zubay, G. Biochemistry / G. Zubay. - 3rd ed . - Wm. С Brown Publishers, 1993. - 1024 p.



